Relativité des normes…
La littérature est abondante sur les normes de volume et de masse ventriculaire gauche et les valeurs proposées sont variables selon les études car elles sont dépendantes de multiples facteurs :
Facteurs physiologiques :
– Taille et surface corporelle ++, de sorte qu’il vaut mieux, en pratique s’exprimer en valeur indexée
– Sexe : valeurs plus élevées chez l’homme
– Age : valeurs plus élevée entre 20 et 45 ans que après 45 ans
– Ethnie (africains > hispaniques > caucasiens > asiatiques)
– Entraînement physique : athlètes VTD + 21%, MVG +42% (Petersen, Scharhag)
Facteurs méthodologiques :
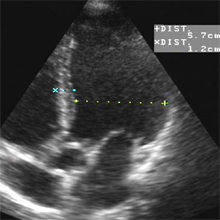
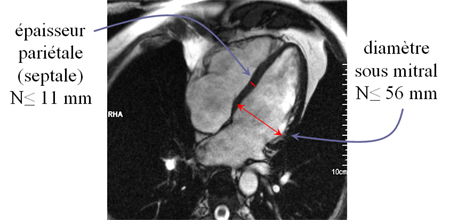
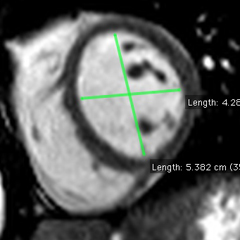
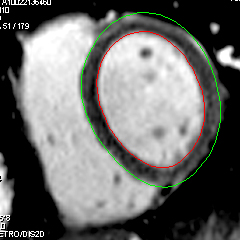
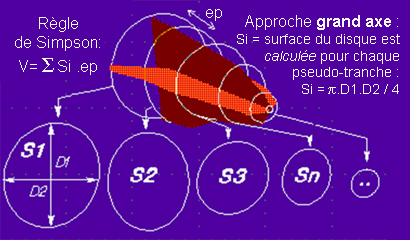
– Mesures sur des coupes grand axe (radiaires) ou petit axe (préférable) – cf: voir infra.
– Volumes et MVG avec écho de spin (BB) > GRE > SSFP
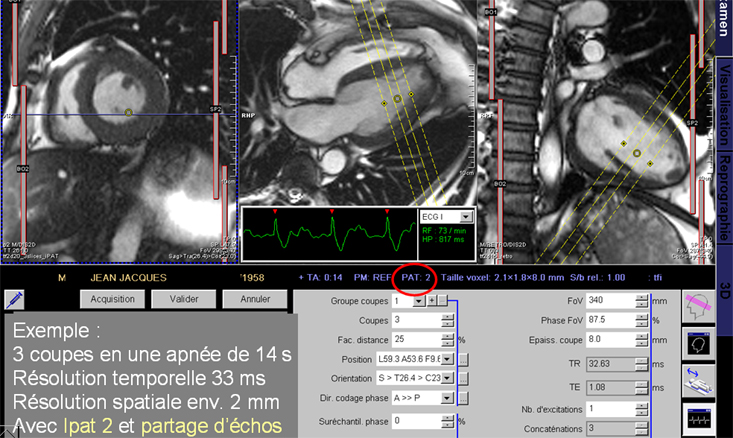
– Partage d’échos tend à sous estimer les volumes et FEVG
– avec ou sans apnée et selon que l’apnée est inspiratoire ou expiratoire
– selon que l’on exclut ou non les piliers des contours endocardiques (9,6%)
Normes proposées par la littérature
Le tableau ci-dessous résume les valeurs proposées par différents auteurs pour les index de volume télédiastolique et de masse VG, étudiés en coupes petit axe.
Les valeurs de volume éjecté (stroke volume) et de fraction d’éjection (FEVG) n’ont pas été reportées dans le tableau pour ne pas le surcharger. Le volume d’éjection systolique est de l’ordre de 50 à 60 ml/m2 chez l’homme et de l’ordre de 40 à 50 ml/m2 pour la femme. Les normes de FEVG sont uniformes entre les auteurs : N = 56 à 75 %.
| Auteur [ref] | Technique | N | IVTD (H) | N< | IVTD (F) | N< | IMVG (H) | N< | IMVG (F) | N< |
|---|---|---|---|---|---|---|---|---|---|---|
| Ciné écho de gradient | non SSFP | |||||||||
| Lorentz 1999 | GRE/PA | 75 | 69.5±11.3 | 92 | 61.0±10.0 | 81 | 91.5±10.8 | 113 | 79.0±8.0 | 95 |
| Standstede 2000 | GRE (age<45) | 18 | 66.0 | 60.0 | 79.0 | 64.0 | ||||
| Standstede 2000 | GRE (age>45) | 18 | 52.0 | 53.0 | 77.0 | 66.0 | ||||
| Salton 2002 | GRE | 142 | 58.0 | 50.0 | 78.0 | 61.0 | ||||
| Marcus | GRE | 73.1±10.9 | 94.9 | 62.2±11.6 | 85.4 | |||||
| Alfaki 2005 | GRE/PA | 60 | 74.4±14.6 | 103.6 | 70.9±11.7 | 94.3 | 77.8±9.1 | 96.0 | 61.5±7.5 | 76.5 |
| Natori 2006 | GRE/PA | 800 | 74.0±15.0 | 104.O | 64.5±11.0 | 86.5 | 85.0±15.0 | 115.0 | 67.0±11.0 | 89.0 |
| Ciné écho de gradient | SSFP | |||||||||
| Petersen 2006 | SSFP/PA | 38 | 89.0±10.0 | 109.0 | 80.0±10.0 | 100.0 | 66.0±9.0 | 84 | 52.0±9.0 | 70.0 |
| Alfakih 2005 | SSFP/PA | 60 | 82.3±14.7 | 111.7 | 77.7±10.8 | 99.3 | 64.7±9.3 | 83.3 | 52.0±7.4 | 66.8 |
| Clay 2006 | SSFP/PA | 16 | 82.5±17.8 | 118.1 | 64.9±11.1 | 87.1 | ||||
| Turbo spin-écho | (black-blood) | |||||||||
| Clay 2006 | TSE BB | 16 | 78.9±32.1 | 143.1 | 77.0±14.5 | 106.0 |
IVTD= index de volume télediastolique (ml/m2), IMVG=index de masse ventriculaire gauche en g/m2. N correspond au nombre de patients étudiés. En bleu les normes pour les homme et en rose, les normes pour les femmes. N< indique le seuil maximal de normalité, défini par la moyenne + 2 écart types (c’est à dire comportant 95% de la distribution).
| Au total, on constate donc des variations considérables : |
| * Selon la méthode IRM utilisée (volumes VG plus grands et masse VG plus petite en SSFP qu’en écho de gradient classique) |
| * Et surtout entre normes échographiques et IRM (MVG normale < 120 g/M2 en écho TM vs 90 en IRM SSFP !) |
| Par conséquent, IL NE FAUT PAS CHERCHER A COMPARER LES RÉSULTATS ECHOGRAPHIQUES ET IRM… |
Variabilité des mesures
La variabilité des mesures a été étudiée notamment par :
– Bottini (1995) qui rapporte des écarts moyens de sur la masse VG (2mesures séparées distantes) de ±8 g en IRM versus 49 g en échographie TM
– Alfakih 2004 qui rapporte un écart type des différences intra-observateur de 9.2 g en IRM vs 24 g en écho 2D
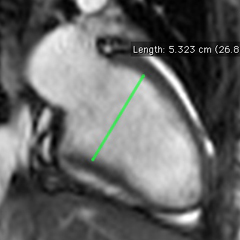
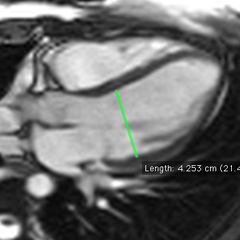
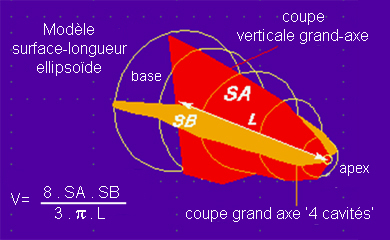
Volumes VG plus grands avec l’approche grand-axe ‘surface-longueur’
Dans notre expérience, chez 46 patients sans anomalie de contraction segmentaire, les volumes ventriculaires sont nettement plus grands en utilisant la méthode 2D à partir de coupes grand axe avec le modèle surface-longueur qu’en utilisant la volumétrie 3D basée sur une pile de coupes petit axe :
| N=46 | VTD (ml) | VTS (ml) | VES (ml) | FEVG (%) |
|---|---|---|---|---|
| Petit axe | 136.7±51.5 | 61.6±37.4 | 75.1±22.7 | 57.1±10.2 |
| Grand axe | 176.3±60.0 § | 66.8±45.0 § | 109.4±34.3 § | 64.1±12.4 § |
| Flux aortique | 83.2±20.6 |
(§ indique un p < 0.005 vs mesures petit axe).
Il convient donc d’être assez réservé quant à l’utilisation de la méthode surface-longueur en grand axe ; la méthode 3D petit axe étant vraisemblablement plus proche de la ‘vérité’ compte tenu de son assez bonne concordance avec la fluximétrie aortique pour définir le volume d’éjection systolique (83.3±23.0 ml en fluximétrie vs 78.7± 21.5 ml en volumétrie chez 146 patients étudiés dans notre centre avec r=0.87).
Normes personnalisées
Si possible, il est recommandé d’établir les normes de son propre centre. Nous avons effectué ce travail chez 44 hommes et 21 femmes (42±15 ans), en utilisant la méthode la plus habituelle qui consiste à réaliser une pile de ciné petit axe en séquence SSFP, en excluant les piliers de la mesure et en retenant les valeurs indexées. Dans ces conditions, nos normes utilisées en pratique de routine sont :
| IVTD (H) | N< | IVTD (F) | N< | IMVG (H) | N< | IMVG (F) | N< |
|---|---|---|---|---|---|---|---|
| 66.0±12.3 | 95 | 61.5±13.2 | 90 | 70.2±10.8 | 92 | 64.5±11.2 | 88 |
IVTD= index de volume télédiastolique (ml/m2), IMVG=index de masse ventriculaire gauche en g/m2. En bleu les normes pour les homme et en rose, les normes pour les femmes. N< indique le seuil maximal de normalité, défini par la moyenne + 2 écart types (c’est à dire comportant 95% de la distribution).
Nota : si l’on souhaite ne retenir qu’un seul chiffre approximatif correspondant à la limite supérieure de la normale pour les index de volume et de masse VG, ce sera 90…
En pratique, nous utilisons ces normes pour établir les compte-rendus d’examen de routine, à l’aide du tableau Excel ci-dessous (téléchargeable en cliquant ici [1]) :